我院劉波主任團隊發表文章榮獲年度高影響力論文獎
由中山大學附屬第三醫院嶺南醫院肝膽胰脾外科劉波主任團隊聯合中山大學生物醫學工程學院劉杰教授團隊在國際知名期刊Acta Pharmaceutica Sinica B(IF=14.6,中科院1區)發表的題為“Bilayer hydrogel dressing with lysozyme-enhanced photothermal therapy for biofilm eradication and accelerated chronic wound repair”的研究成果,于近日被期刊評選為2024年度高影響力論文。文章發表于2023年,針對臨床中常見的慢性傷口不愈合難題而開展,揭示了感染性細菌生物膜在慢性傷口形成中發揮的作用,并且提出了一種通過載藥水凝膠敷料聯合光熱治療消除生物膜、促進傷口愈合的新策略。

圖1 文章獲獎信息
?
慢性不愈合傷口是全球性的健康難題。當慢性傷口合并感染時,傷口組織中大量的細菌及其分泌的胞外聚合物可以形成類似防護屏障一樣的生物膜,其堅固和致密的物理結構特點往往使常規抗菌藥物難以滲透發揮殺菌作用,而機械清除生物膜又會不可避免地破壞傷口周圍組織,且極易復發。光熱治療(PTT)近年來在消除生物膜的研究和應用中逐漸嶄露頭角。然而,由于正常組織對高溫不耐受,針對傷口的PTT療效也受到一定限制,加之光熱元件在傷口表面難以被合理儲存和持續遞送,當前基于PTT的生物膜清除以及促進慢性傷口修復策略效果仍不理想。
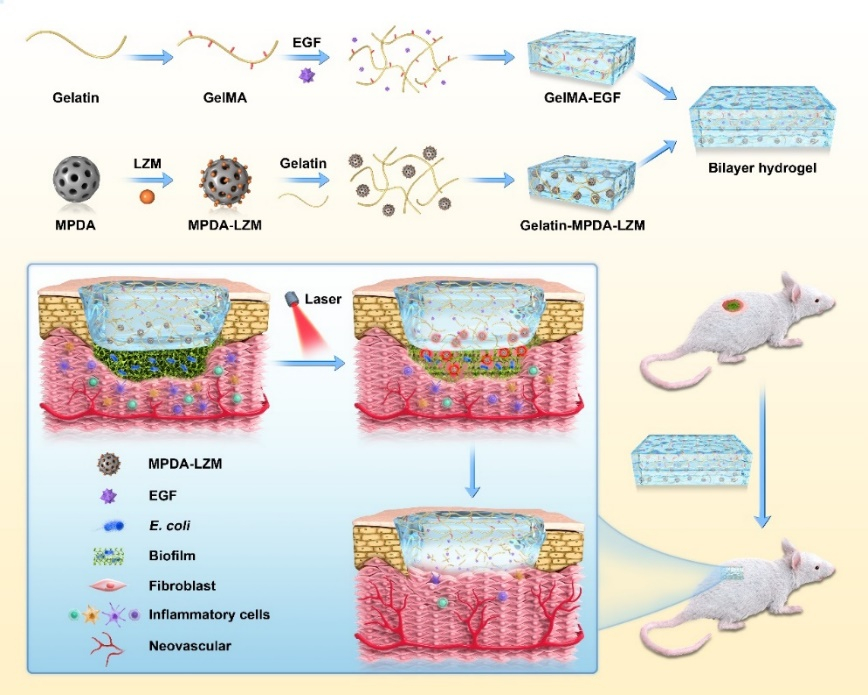
圖2 雙層水凝膠敷料的制備過程及其清除生物膜促進傷口愈合的示意圖
?
鑒于此,團隊聯合開發了一種基于甲基丙烯酸酰化明膠/明膠(GelMA/Gelatin)的雙層水凝膠敷料,分層裝載表皮生長因子(EGF)和介孔聚多巴胺-溶菌酶(MPDA-LZM)納米顆粒。以實現破壞生物膜,殺滅殘留細菌及促進表皮再生等多功能一體化的序貫治療,解決慢性傷口修復難題。雙層水凝膠敷料應用于傷口后,貼合于組織表面的明膠層所負載的MPDA-LZM納米顆粒在近紅外光激發下升溫,使明膠發生熱可逆的固—液轉換而大量釋放納米顆粒,隨即通過PTT作用滲透、破壞生物膜,并將溶菌酶送至生物膜深處殺菌,從根源上消滅細菌,阻止生物膜復發。在一系列的抗感染作用后,穩定強韌的GelMA水凝膠層通過EGF緩釋促進組織再生和傷口再上皮化,進而加速慢性傷口愈合,達到對慢性傷口的階段性分級治療。本研究制備的新型雙層水凝膠敷料在體外實驗中表現了出色的生物膜清除功效,亦在動物模型應用中顯著促進了小鼠嚴重感染性生物膜傷口的愈合,且具備良好的生物相容性。為慢性感染性不愈合傷口的臨床治療提供了一種創新可行的轉化策略。
?
文章鏈接:
https://doi.org/10.1016/j.apsb.2022.03.024









